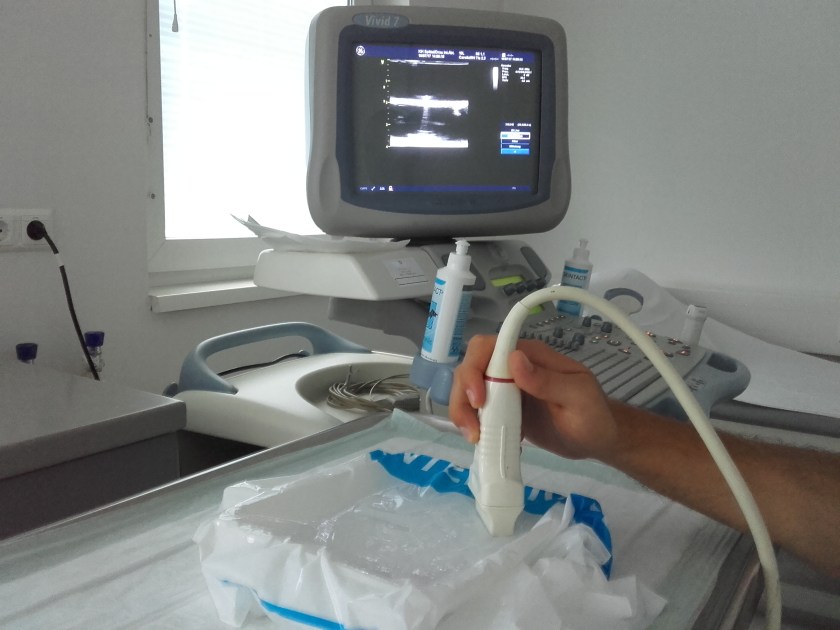
Ich darf euch in diesem Beitrag über meine Zeit in Johannesburg, Südafrika berichten, wo ich im Trauma Unit eines der größten Krankenhäuser arbeiten durfte.
Wenn man das erste Mal in ein Krankenhaus geht um dort zu arbeiten, dann sind die ersten Eindrücke und das Bauchgefühl oftmals entscheidend für die weitere Arbeit. Leider bin ich gleich an meinem ersten Tag 5 Minuten verspätet zur Übergabe gekommen und dementsprechend begrüßt worden. Soviel zum ersten Eindruck, aber im Nachhinein war das deshalb wichtig, da die Übergabe dort eigen und aufgrund der vielen Patienten lange ist. Sie beginnt im Schockraum (16 Betten, alle beatmungsfähig und aufstockbar mit LODOX), zieht über die Trauma Pit (Akutaufnahme vital nicht bedrohter) zur Ward (ca. 50 Betten in einem Raum…) und endet im Konferenzraum, in dem nochmals die Vorkommnisse der letzten 24 Stunden besprochen werden und der Plan für den kommenden Tag mitgeteilt wird. Zeit ist ein extrem wichtiger Faktor in der Traumaversorgung und noch wichtiger wird er, wenn man sie eigentlich gar nicht hat, wie in diesem Krankenhaus, denn die Patienten kommen unentwegt herein, besonders am Wochenende. Nicht nur Zeit ist quasi nicht vorhanden, sondern auch Personal. Die Pflege ist dort eine stolze Gruppe selten arbeitender Menschen, bei denen man sich rechtfertigen muss, wenn man etwas braucht. Nicht weil sie besorgt um die Patienten sind, sondern weil es Arbeit für sie bedeutet. So schlimm das auch klingen mag, entspricht es leider der Wahrheit und drückt den Frust aus, der sich im Laufe der arbeitsreichen Zeit deswegen angesammelt hat. Frustriert vom System, schlecht bezahlt und chronisch überarbeitet macht es aber leider Sinn, dass das so ist. Natürlich bestätigen Ausnahmen die Regel, aber eine brav arbeitende Pflegekraft ist eben nicht genug, wenn man auf einmal mehrere Schwerverletzte im Schockraum zu versorgen hat. Weiters mangelt es an Materialien. So kann es leicht passieren, dass man sich plötzlich mitten in der Versorgung für mehrere Minuten auf die Suche nach Dingen begeben muss, die man eigentlich bereits vor einer Stunde gebraucht hätte – willkommen in Afrika. Ständig wird man im Schockraum nebenbei von der Hintergrundmusik der zahlreichen Alarme begleitet, egal ob Oxylog oder Monitor – Stille erlebt man dort nie! Das Schlimme ist dabei nur, dass es dort jedem mittlerweile egal geworden ist. So kann man es öfter erleben, dass ein Patient seit Minuten asystol geworden, der Sauerstoff aus oder der Patient massiv tachykard ist. Ich habe dort Alarme gesehen, von denen ich nicht einmal wusste, dass es sie gibt.
Das, woran es sicher nicht mangelt, sind die Patienten. Nach einer abendlichen Messerstecherei, Schießerei oder einem Minibustaxi-Unfall, das wieder einmal maßlos überfüllt war, kommen die Patienten alle auf einmal hinein, sodass man sehr geübt in Triage wird. Wie man aus diesen Zeilen herauslesen kann, so muss man sich zunächst hauptsächlich mit dem System und dessen Fehlern herumschlagen, bevor man sich überhaupt um den Patienten kümmern kann.
Die Unit wir komplett von Traumasurgeons geleitet – Vor- und Nachteil zugleich, denn einerseits zieht sich das Management von der ersten Minute bis zur Entlassung von dieser Fachdisziplin durch und die Chirurgen zieren sich nicht mit dem Messer, so bekommen die Patienten sehr schnell Interventionen, bei denen andere eventuell länger über die Indikation nachdenken würden (Koniotomie, Thorakotomie, etc.). Andererseits wird zum Beispiel auch das Airway-Management durch sie durchgeführt, was nicht immer einfach ist, besonders da zu allem Überfluss keine Kapnometrie dort existiert.
Die Patientenversorgung im Schockraum ist standadisiert, so bekommt jeder Patient dort 2 große Leitungen und jeweils einen Liter Hartmann’s solution angehängt (da es keine Stöpsel für die Leitungen gibt), einen eFAST, eine BGA, eventuell einen Harnkatheter und einen zentralen Zugang – innerhalb kurzer Zeit. Die Umsetzung ist leider meist nicht so strukturiert, die Kommunikation großteils übel, aber dennoch funktioniert es – sollte aber kein Maßstab sein.
Aufgrund von eben diesen Fehlern muss man oftmals die eigene Ethik massiv in Frage stellen, denn wenn der Patient wieder einmal ohne Analgetikum eingeleitet wurde und nach wenigen Minuten sich zu wehren beginnt, dann gibt es nun einmal keinen Perfusor, sondern er wird am Bett festgebunden.
Wenn man das alles als Herausforderung sieht, den Idealismus nicht über Bord wirft und sich auf die unglaublichen Traumafälle konzentriert, dann kann man lernen ohne Ende, denn es gibt in der eigenen Vorstellungskraft wirklich nichts, was man dort nicht sehen könnte. Messerstichwunden, Schussverletzungen, Verbrennungen, SHT’s etc. werden sehr schnell „langweilig“, weil man das so oft am Tag zu sehen bekommt, dass das Management in Blut und Knochen übergeht. Der „Arbeitsag“ ist nebenbei auch sehr speziell, denn er dauert mindestens 24 Stunden. Deshalb mindestens, weil nach den 24 Stunden erst die Übergabe für den nächsten Tag beginnt, an der man auch teilnimmt. Anschließend betreut man weiterhin die offen gebliebenen Patienten und kommt dann frühestens nach 26 Stunden aus dem Krankenhaus um am nächsten Tag wiederzukommen.
Hauptsächlich kann ich von meiner Arbeitszeit dort folgende Dinge mitnehmen:
- Schätze den Standard, den du Zuhause gewohnt bist, denn das ist bei weitem nicht selbstverständlich!
Gerade in Europa, wo die Pflege sehr gut ausgebildet und motiviert ist, die entsprechenden Materialien verfügbar sind um Patienten versorgen zu können etc. kann man sich voll und ganz auf die Arbeit am Patienten konzentrieren, was für diese eine immense Sicherheit bedeutet. Viele kleine Probleme erscheinen nach diesem Erlebnis quasi lächerlich. Besonders im Vergleich zu meinen Erfahrungen in Australien ist dieses Abenteuer sehr kontrastreich gewesen. - Praktische Erfahrungen
Die Theorie kann noch so durchdacht sein, wenn in der Praxis die Umsetzungsmöglichkeiten einfach fehlen. Da aber jeder zweite Patient eine Thoraxdrainage, einen zentralvenösen Zugang etc. gebraucht hat, kann man das wirklich extrem gut lernen (unter Vernachlässigung von Sterilität)! - Management und Improvisation
Nachdem so viele Patienten wellenartig eingetroffen sind, lernt man zwangsläufig mit dieser Flut umzugehen. Improvisation ist dabei alles, denn wenn Materialien/Personal etc. fehlen, kann man lebenserhaltende Prozesse dem Patienten dennoch nicht vorenthalten. - Priorisierung eigener Moral
Es kann sehr leicht passieren, dass man in das Hamsterrad dieses Systems aufspringt und einem vor Schmerz schreiende oder am Tubus-kauende Patienten, Alarme oder die Suche nach Materialien schnell „egal“ werden, besonders wenn man nach 20 Stunden unentwegtem Arbeiten wieder einer Patientenflut entgegensteht. Mehr denn je wird es da wichtig zu reflektieren und sich darauf zu besinnen, warum man sich diesen „Zirkus“ eigentlich antut. Das ist eine der zentralsten Fragen überhaupt, die jeden trifft – dort wird man dazu gezwungen. Entweder man ignoriert das und wird zu einer Maschine, die irgendwann am fehlenden Öl – der Motivation – zerbricht oder man findet in der Antwort unerschöpfliche Lust an der Arbeit mit Menschen, it’s up to you!