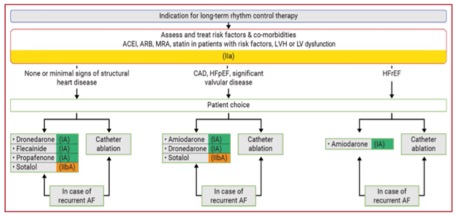
Vor kurzem erschien die neue Leitlinie der Europäischen Gesellschaft für Kardiologie zum Thema Akutes Koronar Syndrom (ACS). Zum Zwecke dieses Beitrages habe ich den Fokus auf die Präklinik gelegt. Ihr kommt also nicht darum rum, die Guidelines selbst zu lesen 😉
Was hat sich getan? Ein paar wenige Neuerungen gibt es schon, aber vor allem für den präklinischen Bereich bleibt auch vieles gleich.
Kurz was ist wissenswert:
- Direkt in ein Herzkatheterlabor sollen Patienten kommen mit entsprechenden klinischen Symptomen sowie STEMI (-Äquivalenten) bzw. mit very-high risk features im Rahmen eines NSTE-ACS.
- Präklinisches Loading mit einem P2Y12-Rezeptor Hemmer wurde downgegraded
- Falls doch: Prasugrel bevorzugen
- Routinemäßig sollten aber Patienten nach einem HKS nicht angiographiert werden, sondern nur dann, wenn sich eine persistierende ST-Hebung (oder ein STEMI Äquivalent) zeigt.
Was für viele ein Paradigmenwechsel ist, ist die Tatsache, dass es nun eine Leitlinie für das gesamte Spektrum des ACS gibt. In den vorangegangenen Leitlinien wurde immer zwischen ST-Elevation und Nicht-ST-Elevation unterschieden (und vor allem auch dyssynchron publiziert).
Hier wird nun erstmalig von einem Spektrum im Rahmen des ACS gesprochen:

Wann muss ich nun an ein ACS denken? Dann:
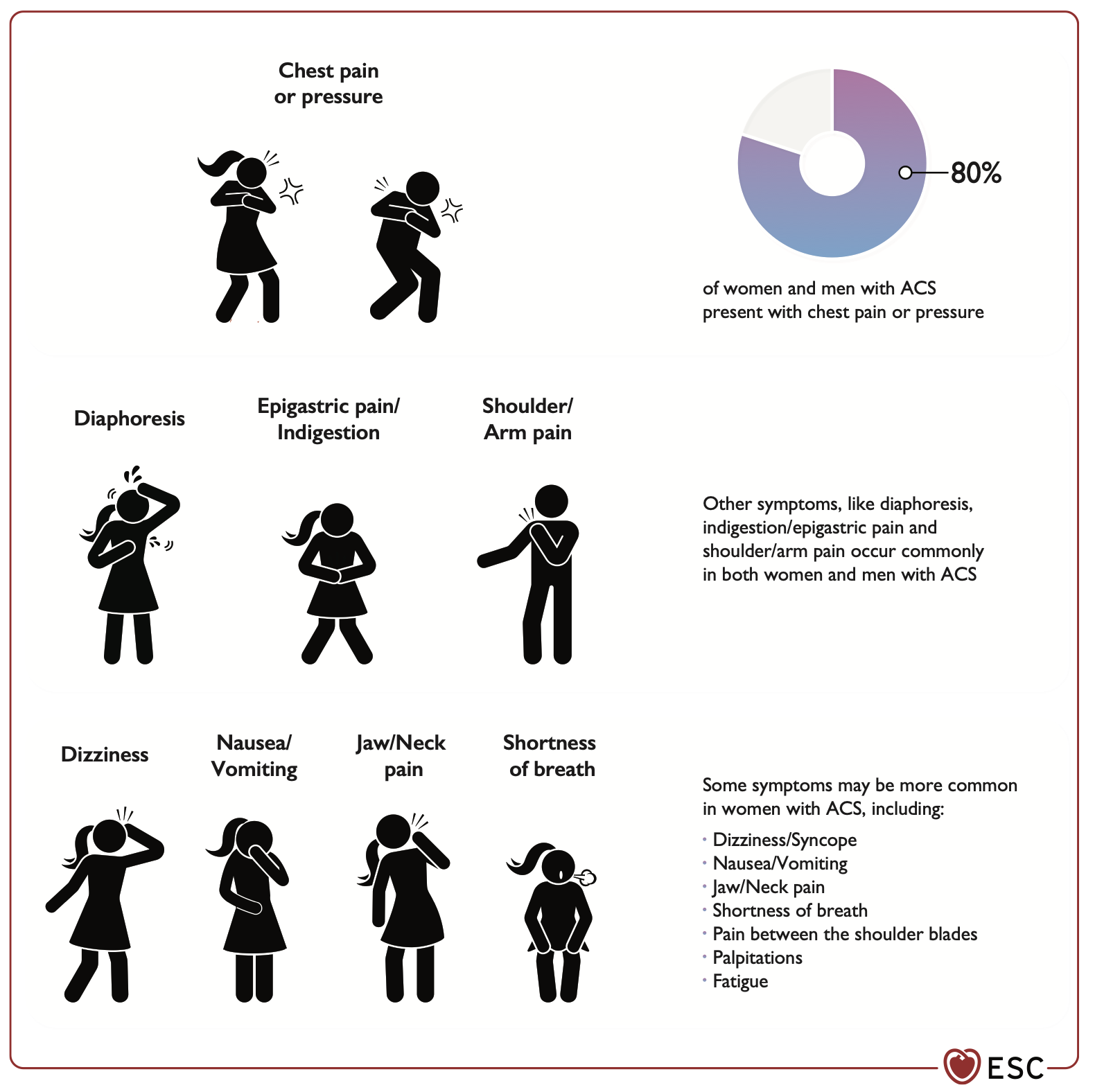
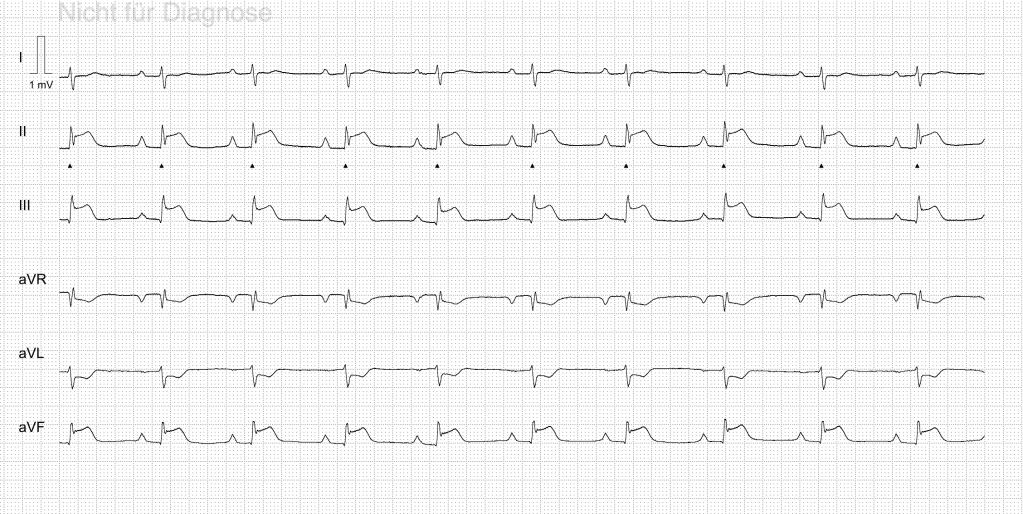
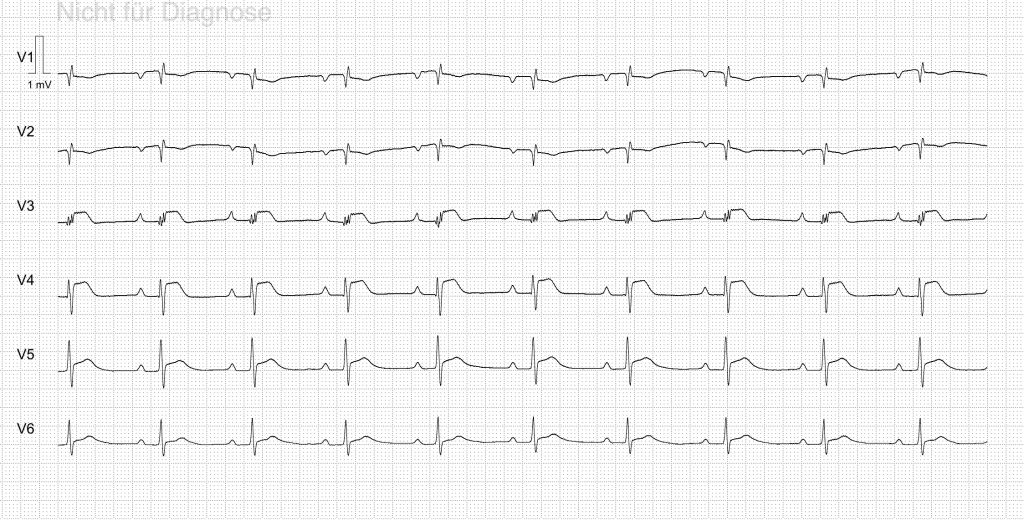
Danach sollte so bald wie möglich (< 10 Minuten) ein 12-Kanal EKG geschrieben (und richtig interpretiert) werden.
Hier wird dann in 2 Arbeitsdiagnosen unterteilt.
Patienten mit akutem Brustschmerz (oder äquivalenten Symptomen) und der Arbeitsdiagnose
- ST-Strecken-Hebung MI: STEMI
- Nicht-ST-Strecken-Hebung [NSTE]-ACS.
Ad 1) MI: STEMI
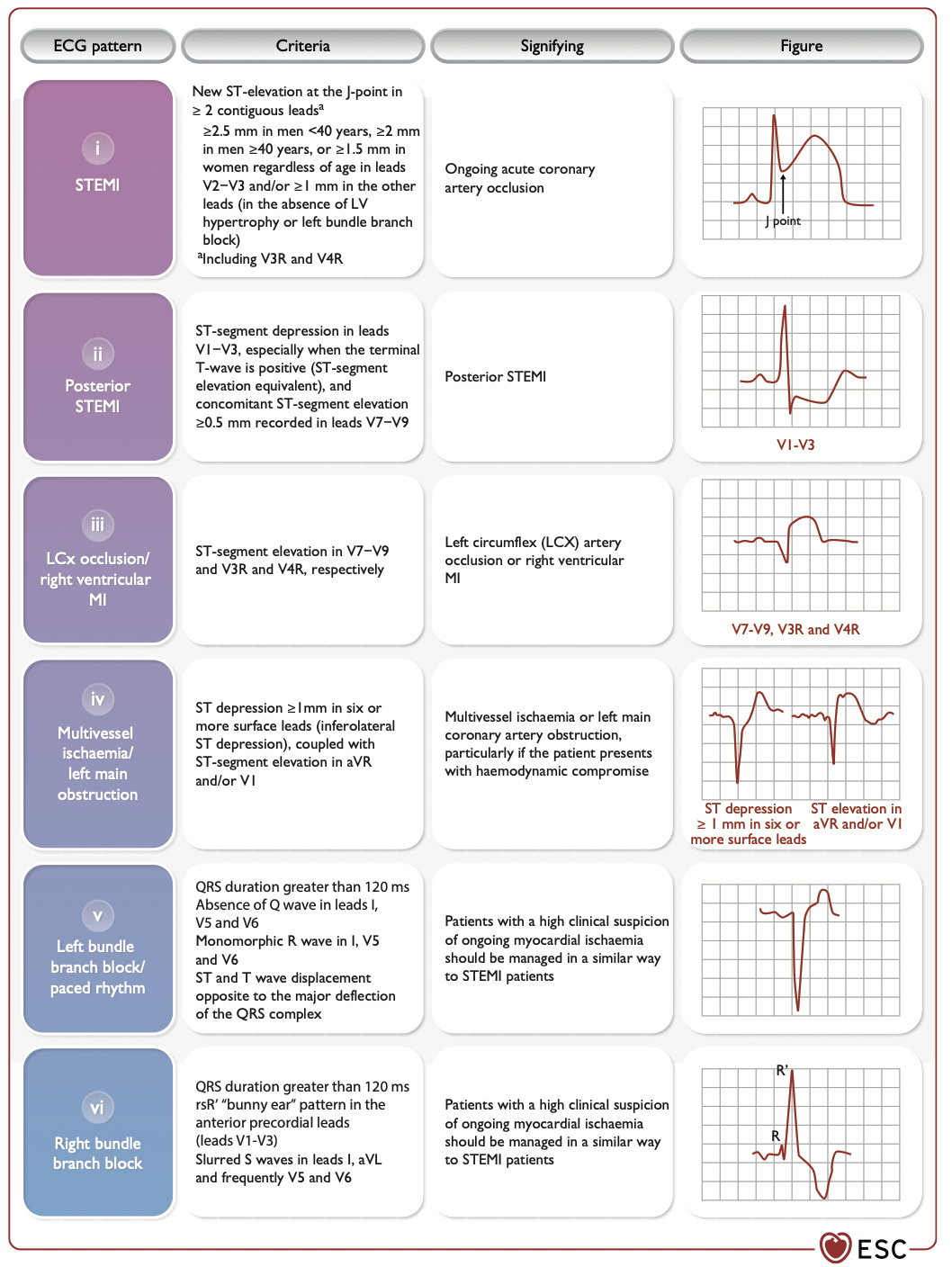
bzgl. Schenkelblockbilder.
Sgarbossa Kriterien (auch andere Kriterien werden zumindest zitiert) helfen, die Patienten rauszufiltern, welche von einer sofortige Koronarangiographie profitieren. Alles natürlich bei entsprechender Klinik. Ein LSB ist für sich allein genommen ist kein Hinweis auf einen aktuell vorliegenden Koronararterienverschluß.
- Bei mehr als 50 % der Patienten, die mit Brustschmerzen und LSB in die Notaufnahme kommen wird schlussendlich eine andere Diagnose als ein Myokardinfarkt gestellt.
- Bei weniger als 40 % der Patienten, die mit Brustschmerzen und RSB in die Notaufnahme kommen, wird letztendlich ein MI diagnostiziert.
- Bei Patienten mit RSB sind ST-Senkungen in I, aVL, V5 und V6 jedoch hinweisend für ein NSTE-ACS.
Wie immer bei gilt: auf die Klinik achten, falls vorhanden mit Vor-EKGs vergleichen und serielle EKGs schreiben!
Ad 2) Nicht-ST-Strecken-Hebung [NSTE]-ACS.
Das heißt:
- unauffälliges EKG
- vorübergehende ST-Strecken-Hebungen
- anhaltende oder vorübergehende ST-Streckensenkungen
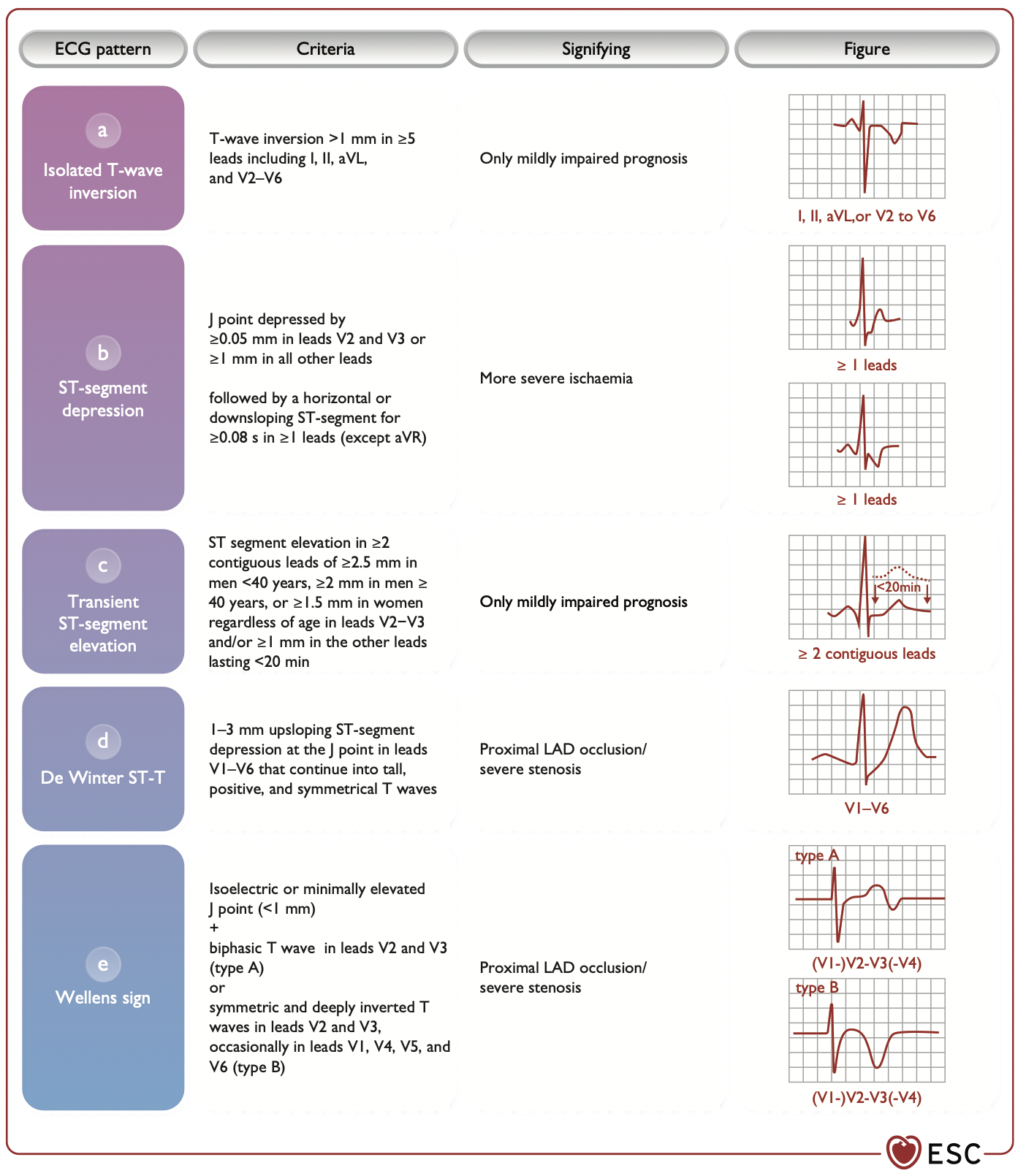
- T-Wellen-Anomalien (z.B. hyperakute T-Wellen, T-Wellen-Inversion, biphasischer T-Wellen, flache T-Wellen und Pseudo-Normalisierung)
Hierunter werden auch das Wellens-Syndrom und die de Winter T-Wellen genannt.
Was sind nun EKG-Äquivalente die direkt ins Herzkatheterlabor bzw. in ein Zentrum mit PCI Möglichkeit kommen?
Patienten mit
- STEMI-(Äquivalenten) und Ischämiesymptomen < 12 Stunden
- very high und high Risk NSTE-ACS (Definition siehe Abbildung)
- Patienten die präklinisch lysiert worden sind (indiziert falls ein PCI Zentrum nicht innerhalb von 120 Minuten erreicht werden kann, was in unserem System ja eine Ausnahme sein sollte)

Akuttherapie (für Patienten, die nicht oral antikoaguliert sind oder lysiert werden):
- Sauerstoff: Bei einer SpO2 < 90%
- Nitrate (cave bei Hypotension, PDE-5 Hemmer, RV-Beteiligung)
- Morphin bei Schmerzen. Auch wenn es Diskussion bzgl. Resorption, Plättcheninteraktion etc. gibt, werden Opioide empfohlen (IIa/C)
- Milder Tranquilizer: bei sehr ängstliche Patienten
- i.v. Betablocker: vorzugsweise Metoprolol, falls eine PPCI geplant ist. (cave akute Herzinsuffizienz und Hypotension)
- Acetylsalicylsäure: 75–250 mg i.v.
- Heparin unfraktioniert 70-100 IE/kg
- Präklinisches Loading mit einem P2Y12-Rezeptor-Hemmer?
wurde downgegraded:

Es gibt keinen klaren Beweis aus großen Studien dafür, dass es sinnvoll ist, P2Y12-Rezeptor-Inhibitoren routinemäßig vorab zu verabreichen. Bei einem NSTE-ACS sollte man präklinisch sowieso nicht loaden. Erst dann, wenn man die Koronaranatomie kennt.
Immer wieder kommt es vor, dass Patienten mit einem P2Y12 Hemmer geloaded werden, die dann doch eine Akut-Bypass OP brauchen oder eine Aortendissektion haben. Eine große Downside gegenüber einer geringen Upside.
Falls man sich dennoch dazu entschließt, sollte Prasugrel (60 mg) bevorzugt werden (bessere Daten bzgl. Tod, Herzinfarkt oder Schlaganfall ohne Zunahme von Blutungskomplikationen. (ISAR-REACT Studie).
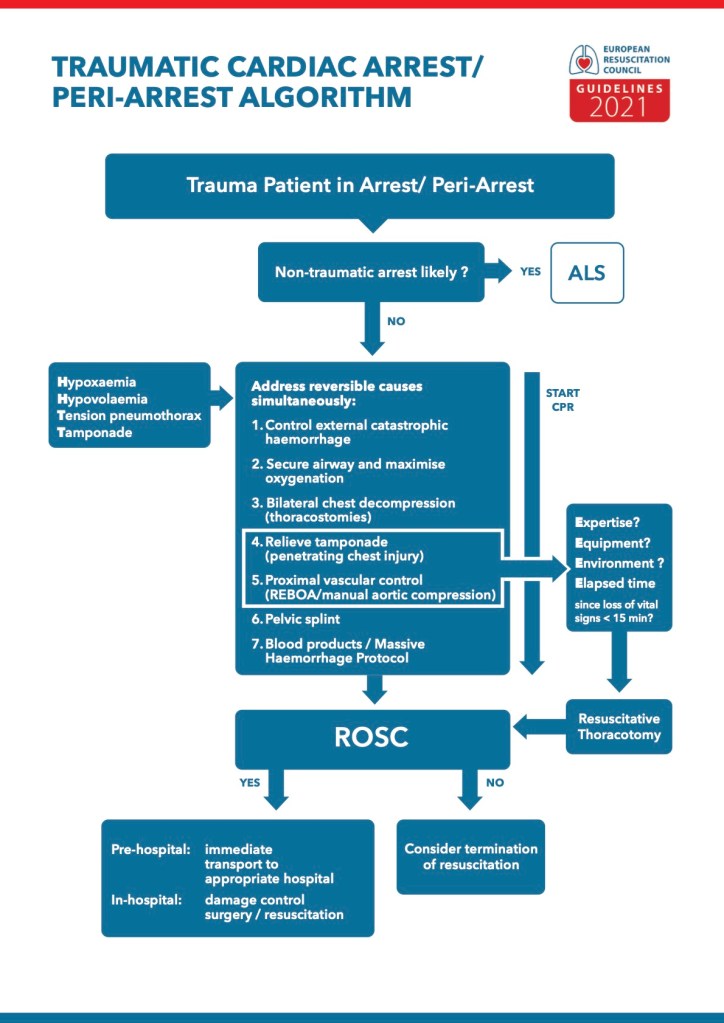
ROSC
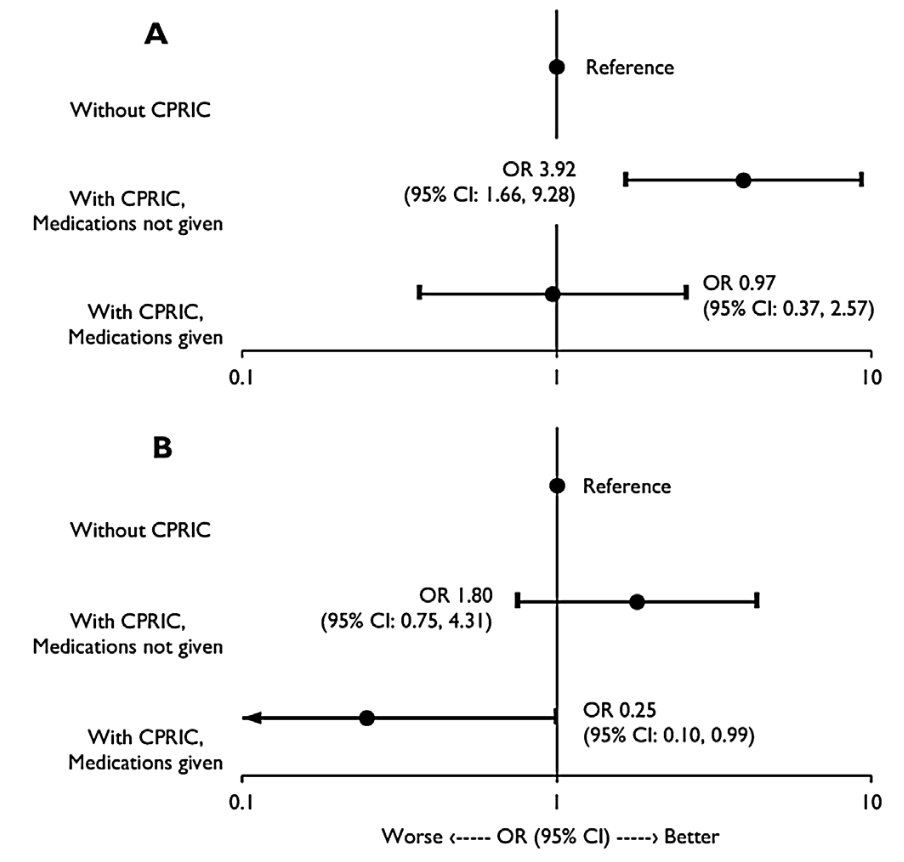
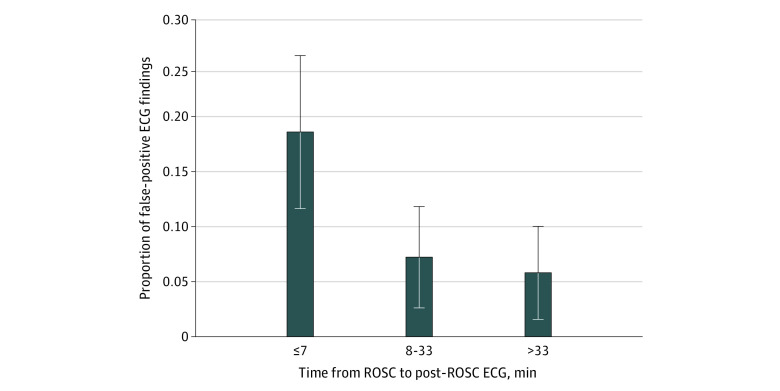
Wie wir alles wissen, ist das akute Koronarsyndrom die häufigste Ursache für einen präklinischen Herzkreislaufstillstand. Routinemäßig sollten aber Patienten nach einem HKS nicht angiographiert werden, sondern dann, wenn sich eine persistierende (> 20 Minuten) ST-Hebung (oder ein STEMI Äquivalent) zeigt. Bei initial schockbarem Rhythmus ohne ST-Elevation (oder Äquivalent) und ohne kardiogenem Schock bringt eine sofortige invasive Koronarangiographie keine Vorteile und soll im weiteren Aufenthalt reevaluiert werden. Der Fokus in dieser Phase sollte sich auf den Ausschluss nicht-koronarer Ursachen konzentrieren (zerebrovaskuläre Ereignisse, respiratorische Insuffizienz, nicht-kardiogener Schock, Lungenembolie oder Intoxikation). Alles in Zusammenschau mit hämodynamischer/elektrischer (in)Stabilität und Neurologie.

Quelle und Abbildungen:
2023 ESC Guidelines for the management of acute coronary syndromes: Developed by the task force on the management of acute coronary syndromes of the European Society of Cardiology (ESC)
Link