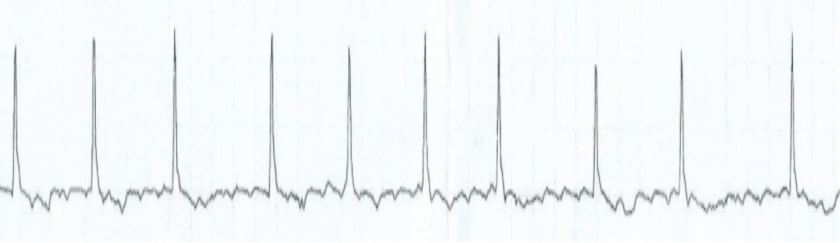
Regellos arrhythmisch? Schmal? Tachykard? Ohne P-Wellen? – Ganz klar, das EKG zeigt den typischen Befund einer Vorhofflimmerarrhyhtmie. So weit so gut, aber was ist nun zu tun? Die einfach gestellte Diagnose kann in der einen Situationen rasches Handeln mit Kardioversion erfordern und wirft in anderen Fällen bei hämodynamischer Stabilität im Verlauf viele Fragen in der weiteren Diagnostik, Management und Therapie auf…
Vielleicht werden sich einige Fragen, warum die VHFA hier im Rahmen eines Notfall-/Intensiv- oder Anästhesiesettings besprochen wird.
Zum einen ist es so, dass AF (Atrial Fibrillation, Vorhofflimmern) ein häufiges rhythmologisches Problem darstellt (auf der Intensivstation ist es sogar die häufigste Arrhythmie). Andererseits kann es auch zu hämodynamischer Instabilität führen und ist generell mit einer erhöhten Mortalität verbunden.
Initial fällt einem die Diagnostik nicht immer (besonders wenn sehr tachykard oder in Verbindung mit einem Schenkelblock) leicht…
Eine adäquate Therapie in der Akutsituation sowie Evaluation einer notwendigen Schlaganfallprophylaxe, richtige Prognose und Komorbiditätenmanagement sind von medizinisch und volkswirtschaftlich relevanter Bedeutung.
Aus diesen und mehreren anderen Gründen beschäftigte sich 2020 die ESC erneut mit diesem Thema und brachte neue Leitlinie heraus, die hier insbesondere mit dem Augenmerk auf Neuerungen besprochen werden sollen.
CC- ABC
CC steht für Confirm und Characterize AF im Rahmen der Diagnostik. Hierbei wird herausgestrichen, dass es unumgänglich ist vor Therapie der Rhythmusstörung und Einleitung einer etwaigen DOAK Therapie AF als solches zu diagnostizieren. Klingt auf den ersten Blick trivial, ist es jedoch nicht immer. Häufig werden Patienten wegen arrhythmischen Pulses zugewiesen mit der Frage „Arrhythmischer Puls- DOAK Einleitung?“. Ein arrhythmischer Puls bedeutet jedoch keinesfalls zwangsläufig ein AF.
AF muss mittels 12 Kanal EKG oder einem Rhythmusstreifen (hier unbedingt >30sek. dokumentiert) diagnostiziert werden.
Neu ist auch, dass sogenannte „Devices“ wie z.B. Smart Watches, verschiedene Smartphone Apps sowie Rhythmsticks usw. verwendet werden können (Diagnose AF hier ebenfalls auch erst ab dokumentierter Flimmerdauer >30sek.)
Bei dem zweiten C der Diagnostik (Characterize) geht es um die sog. „4S“:
- symptom severity
- severity of burden
- substrate und
- stroke risk.
Mittels EHRA Score soll die Schwere der Symptomatik der einzelnen AF Episoden bestimmt werden. Je häufiger und länger symptomatisches AF besteht desto höher ist die „severity of burden“. Mittels Echokardiographie und ev. weiteren bildgebenden Methoden (z.B. Cardiac MR) sollte das morphologische Substrat (Vorhofgröße, Kardiomyopathie,…) dargestellt und mittels CHA2DS2VASc Risikoscores das Schlaganfallrisiko (stroke risk) abgeschätzt werden.
| Stadium | Schweregrad | Alltagskompetenz |
| EHRA I | Keine Beschwerden | Normale tägliche Aktivität ist nicht eingeschränkt |
| EHRA II | Milde Beschwerden | Normale tägliche Aktivität ist nicht eingeschränkt |
| EHRA III | Schwere Beschwerden | Normale tägliche Aktivität ist eingeschränkt |
| EHRA IV | Massive Beschwerden | Normale tägliche Aktivität ist unmöglich |
Sind diese 4S geklärt, kann abgeschätzt werden wie symptomatisch der/die Patientin ist und welche Therapie (Rhythmus- vs. Frequenzkontrolle) sinnvoll für ihn/sie ist. Das leitet uns zum ABC der Therapie über:
ABC steht für Anticoagulation, better symptom control, cardiovaskular risk factors and comorbidity management.
Bevor wir uns um A wie Anticoagulation oder C wie Comorbidities kümmern ist es in der Akutsituation natürlich von unabdingbarer Bedeutung zu erkennen ob der Patient hämodynamisch instabil ist. Es geht hier also im Real-Life-Setting zunächst um das B (better symptom control). Die Frage die wir uns also stellen müssen ist, wie symptomatisch der/die PatientIn im Moment des Eintreffens am Einsatzort/im Krankenhaus ist. Hämodynamische Instabilität bedeutet klarerweise für Rhythmusstörungen eine Indikation für Rhythmisierung mittels elektrischer Kardioversion.
Liegen keine Instabilitätszeichen vor habe ich Zeit mir zu überlegen ob die Symptome des/der Patienten/in überhaupt durch AF bedingt sind, ob eine Antikoagulation einzuleiten ist, wie hoch das Blutungsrisiko ist usw. Hierzu ist dann folgendes zu beachten:
A Anticoagulation
Betreffend die Antikoagulation sind seit Jahren 2 Abkürzungen/Akronyme weiterhin unumstößlich mit AF vergesellschaftet: der CHA2DS2VASc Score zeigt uns das Schlaganfallrisiko an während der HASBLED Score über die Blutungsneigung Auskunft gibt. Ab einem Score von 1 für Männer und 2 für Frauen ist eine (D)OAK Therapie zu erwägen ab 2 für Männer/3 für Frauen auf jeden Fall indiziert. Den DOAKs wird übrigens klar der Vorzug gegenüber VKAs gegeben. DOAKs sind jedoch beim valvulären AF (höhergradige Mitralstenose, Z.n. mech. Klappenoperationen) nicht zu verordnen. Hier besteht die Indikation für VKAs (Vitamin K Antagonisten).
Wird aufgrund der klinischen Symptomatik eine Kardioversion (medikamentös oder elektrisch) angestrebt und die AF Dauer ist sicher <48h, kann sofort eine Rhythmisierung ohne LAA Thrombenausschluss (Thrombus im linken Herzohr) erfolgen. Bei einer Dauer >48h ist entweder eine DOAK Therapie über 3 Wochen mit anschließender Kardioversion gefolgt von zumindest 4 wöchiger (CHA2DS2VASc 0 -1 Männer, 1- 2 Frauen) oder lebenslanger (CHA2DS2VASc≥1 bei Männern, 2 bei Frauen) DOAK Therapie angezeigt. Besteht die Möglichkeit eine TEE (Transösophageale Echokardiographie) vor Kardioversion zum LAA Thrombusausschluss durchzuführen, kann auch ohne initialer DOAK Therapie kardiovertiert werden. Eine anschließende DOAK Therapie ist jedoch je nach CHA2DS2VASc notwendig (siehe oben).
In der speziellen Situation mit gesicherter sehr kurzer symptomatischer Flimmerdauer (<24h) mit bekanntem Auslöser (z.B. Fieber, Alkoholkonsum,..) und niedrigem CHA2DS2VASc (0 für Männer, 1 für Frauen) kann eine Kardioversion ohne TEE und ohne anschließender DOAK Therapie erwogen werden.
Die Guidelines betonen, dass ein relevant hoher HASBLED keine Kontraindikation für eine DOAK Therapie darstellt. Der Benefit durch die Antikoagulation überwiegt oft das Blutungsrisiko und die HASBLED Risikofaktoren sind teilweise durch Therapie und Compliance beeinflussbar. Auf etwaige Blutungsstigmata sollte jedoch besonders geachtet werden.
Sollte es unter DOAKs zu einer Blutungskomplikation kommen ist es wichtig die letzte DOAK Einnahme zeitlich einzuordnen um sinnvolle Schritte setzen zu können. Hämoglobin sowie Thrombozytenzahl, Nierenfunktion und Leberfunktion sollen evaluiert und die DOAK Therapie pausiert werden.
12-24h nach DOAK Einnahme sollte aufgrund der kurzen HWZ (Halbwertszeit) kein relevanter Effekt mehr vorhanden sein. Wurde die DOAK Therapie erst vor 2-4h verabreicht empfiehlt es sich Aktivkohle oder eine Magen-Lavage zu versuchen (falls keine OP im Raum steht). Dabigatran kann (rein theoretisch) außerdem dialysiert werden.
An lokalen Maßnahmen finden sich für kleiner Blutungskomplikationen bei komprimierbaren Wunden die mechanische oder chirurgische Blutstillung. Sollte der V.a. auf eine GI-Blutung bestehen sind auch hier lokal blutstillende Interventionen zu setzen (Gastroskopie)
Bei moderaten Blutungen werden zusätzlich Flüssigkeitssupplementierung und ggf. Erythrozytenkonzentrate empfohlen.
Bei schweren Blutungen unter VKAs wird FFP (Fresh frozen plasma) gegenüber Vitamin K aufgrund schnellerer Wiederherstellung der Koagulationsfähigkeit bevorzugt. Prothrombinkomplexkonzentrate wirken allerdings noch schneller und sind daher als First-line Therapie anzusehen.
Zur Aufhebung der Wirkung von Dabigatran soll Idarucizumab (Praxbind©) und für Faktor Xa Inhibitoren (Xarelto©, Eliquis©,…) Andexanet alfa (Ondexxya©) gegeben werden. Über die Verwendung von Prothrombinkomplexkonzentraten bei Blutung unter Xa Inhibitoren bestehen noch wenige Daten. Dies kann jedoch ebenfalls versucht werden.
Eine praktische Übersicht über das Management der Blutung unter oraler Antikoagulation gibt es hierzu von der Arbeitsgruppe perioperative Gerinnung der ÖGARI.
Insgesamt soll nach Blutungsereignis nicht vergessen werden die Indikation einer weiterführenden DOAK Therapie erneut zu reevaluieren und ggf. wiedereinzuleiten.
Sollte es einmal zu einer lebensbedrohlichen Blutung unter DOAKs gekommen sein, bietet sich noch das interventionelle Verfahren eines Herzohrverschlusses an (weitere Indikationen dafür: Insult unter suffizienter (D)OAK und LAA Thrombus,Dialyse, hoher HASBLED)
B Better symptom control
Die Symptomkontrolle oder better symptom control (B) haben wir weiter oben bereits kurz angesprochen.
Besteht keine für AF typische klinische Symptomatik genügt es eine Frequenzkontrolle einzuleiten (Ziel: Herzfrequenz <110) um einer Tachykardiomyopathie und etwaiger kardialer Dekompensation vorzubeugen. Je nach Begleiterkrankungen kommen unterschiedliche Pharmaka zum Einsatz. Betablocker sind mit Ausnahme einer COPD/Asthma Erkrankung First-Line Therapeutika. Bei COPD/Asthma können Kalziumantagonisten (Diltiazem-/Verapamiltyp) verwendet werden. Als Add-On kommt das altbewährte Digitalis und als letzte Option in dieser Reihe auch Amiodaron in Frage. In speziellen Situationen kann auch eine Ablate and Pace Strategie in speziellen Zentren angewandt werden.
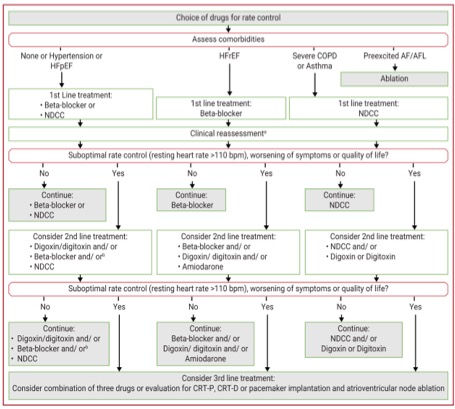
Sind Symptome vorhanden, jedoch nicht zwangsläufig eindeutig AF zuzuordnen sollte zunächst ein Sinusrhythmus hergestellt und anschließend reevaluiert werden. Haben sich die Symptome durch die Kardioversion gebessert wird fortführend eine Rhythmuskontrolle mit AA (Antiarrhyhtmika) oder einer Ablation angestrebt. Für eine das Anstreben einer Rhythmuskontrollstrategie sprechen folgende Faktoren:
- Alter<65J
- Kurze Flimmerdauer
- Tachykardiomyopathie
- Nur ggr. Vorhofdilatation
- Keine oder wenige Komorbiditäten
- Auslösung durch akute Erkrankung
- Schwierige Frequenzkontrolle
- Patientenwille
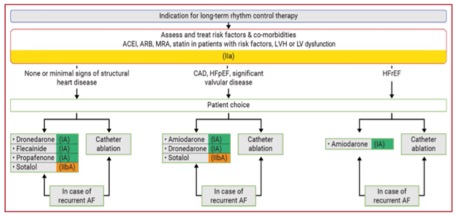
In den ESC 2020 Guidelines hat die Ablation als First-line Therapie zur Rhyhtmuskontrolle beim paroxysmalen AF eine Aufwertung erfahren (II A Empfehlung). Bei paroxysmalem oder persistierendem AF mit HFrEF (Herzinsuffizienz mit reduzierter Ejektionsfraktion) besteht eine Klasse I Empfehlung hinsichtlich einer Ablation als First-line Therapie (reduziert Mortalität und Hospitalisationen). Hier ist jedoch auch auf die Begleitumstände wie LA (linker Vorhof)-Größe usw. zu achten, welche die Erfolgsaussichten einer Ablation determinieren.
Entschließt man sich zu einer medikamentösen antiarrhythmischen Dauertherapie müssen kardiale Begleiterkrankungen beachtet werden. Ist der/die PatientIn „herzgesund“ (keine KHK, keine CMP) können Propafenon oder Flecainid, sowie Dronedaron gegeben werden. Ist der/die PatietIn „herzkrank“ bleiben Amiodaron und Dronedaron als Optionen für die medikamentöse Dauertherapie. Bei HFrEF ist Amiodaron die einzige medikamentöse Option.
C Cardiovascular risk factors and Comorbidity management
Die Leitlinie macht 2020 wieder vermehrt darauf aufmerksam die Begleiterkrankungen des Patienten zu untersuchen und diese auch suffizient zu behandeln. Unter konsequenter Therapie der Begleitumstände (DM, Hypercholesterinämie, Bluthochdruck, OSA, Adipositas, Bewegungsmangel, Rauchen) ist es leichter möglich einen SR herzustellen und zu erhalten. Bei Verdacht ist ein Screening auf Komorbiditäten damit unabdingbar zu empfehlen.
Postoperatives VHFA
Bei 20-50% der kardiochirurgischen Patienten tritt AF postoperativ auf. Nach großen gefäßchirurgischen Operationen und Colorektalen Operationen kommt es immerhin auch in 5-10% der Fälle zu postoperativem AF. Der Großteil der Episoden ist selbstlimitierend, jedoch ist das Risiko für ein Rezidiv 4-5fach erhöht in den nächsten 5 Jahren.
Zur Prävention bei erneutem kardiochirurgischem Eingriff bei Z.n. postoperativem AF sind BB oder Amiodaron zu empfehlen (Ia A)
Betreffend der Antikoagulation gilt zu bedenken, dass ein kardiochirurgischer Eingriff wohl als Stimulus für AF zu werten ist und AF deshalb nicht notwendigerweise nach Ausheilung der Operation weiterbestehen muss.
Aufgrund des Nettobenefits einer (D)OAK Therapie hinsichtlich thrombembolischer Ereignisse gegenüber dem verbundenen Blutungsrisiko im Follow-up (nach Wundheilung mit Absprache mit dem Chirurgen) kann eine (D)OAK Therapiebei post-kardiochirurgischem AF entsprechend dem CHA2DS2VASc angedacht und mit dem Pat. besprochen werden (IIb B). Bei post-nicht-kardiochirurgischen AF sollte sie explizit in Betracht gezogen werden (IIa B Empfehlung)
Vorhofflimmern ist die häufigste Arrhythmie, die auf der Intensivstation auftritt. Diese Situation ist unterscheidet sich jedoch oft von Vorhofflimmern in anderen Zusammenhängen, da ein neu aufgetretenes Vorhofflimmern oft auf physiologischen Stress einer kritischen Erkrankung zurückzuführen ist (Sepsis, Lungenembolie etc.) Mehr hierzu im lesenswerten IBCC Kapitel von Josh Farkas.
—————————————————————————-
Dieser Beitrag wurde geschrieben von Dr. Mario Gruber, Arzt für Allgemeinmedizin, Notarzt und in Ausbildung zum Facharzt für Irreres 😉
Literatur:
2020 Guidelines for Management of Atrial Fibrillation
ESC Clinical Practice Guidelines
Pingback: Nerdwoche am 10.10.2021 – Nerdfallmedizin.de