Dezember 2016
Es ist 04:30 Uhr morgens als uns (4 Besatzungsmitglieder) der Notruf weckt. Wir werden zu einer Wohnung gerufen, in der ein 23a alter Mann laut Mutter schwer erweckbar ist, seit 3 Tagen bereits schläft und „etwas genommen haben soll“.
Zu dieser Uhrzeit fällt es zugegebenermaßen nicht gerade leicht, das als schwerwiegend zu finden, da auch ich um 4:30 Uhr üblicherweise schwer erweckbar bin. Nichts desto trotz machen wir uns auf den Weg und erreichen kurz darauf den Einsatzort, eine kleine Wohnung im Hochparterre, leicht erreichbar und keine Gefahrensituation auszumachen. Ein RTW ist bereits vor Ort, hat begonnen die Vitalparameter zu checken und übergibt uns das. Der erste Eindruck ist alles andere als beruhigend: ein junger Mann, nur mit Boxershorts bekleidet in einem großen Bett liegend, das von 2 Seiten her zugänglich ist, somnolent und unruhig, sobald man Kontakt mit ihm aufnehmen will und zeigt ein blass-grau-marmoriertes Hautkolorit – also blickdiagnostisch OMG+!
Die Überlastungsphase ist angekommen, denn gleichzeitig wird das Monitoring angeordnet, ein i.v. Zugang gelegt, Sauerstoffverabreicht und ich beginne von der Anwesenden – deutlich besorgten – Mutter eine ausführliche Anamnese zu erheben, während ich den Patienten nach dem ABCDE-Schema zu beurteilen beginne. Die Anamnese bestätigt die bisher bekannten Angaben, außerdem erzählt mir die Mutter, dass ihr Sohn zwar eine Drogenvorgeschichte hätte (nicht näher spezifizierbar) und auch vor kurzem im Krankenhaus deshalb war aber diesmal glaubt sie nicht, dass es damit zusammenhängt. Er sei vor 3 Tagen zu ihr gekommen und wollte mit einem Freund etwas unternehmen, es ging ihm aber nicht besonders gut und er hat sich hingelegt – seither war er nicht mehr aufgestanden, hat weder gegessen noch getrunken, das Bett eingenässt und sie habe bereits am Tag 1 den Ärztenotdienst verständigt, dieser sei aber nicht gekommen. Heute früh stellte sie keine Verbesserung fest und hat uns deshalb alarmiert. Der Patient habe keine wesentlichen Vorerkrankungen oder Allergien.
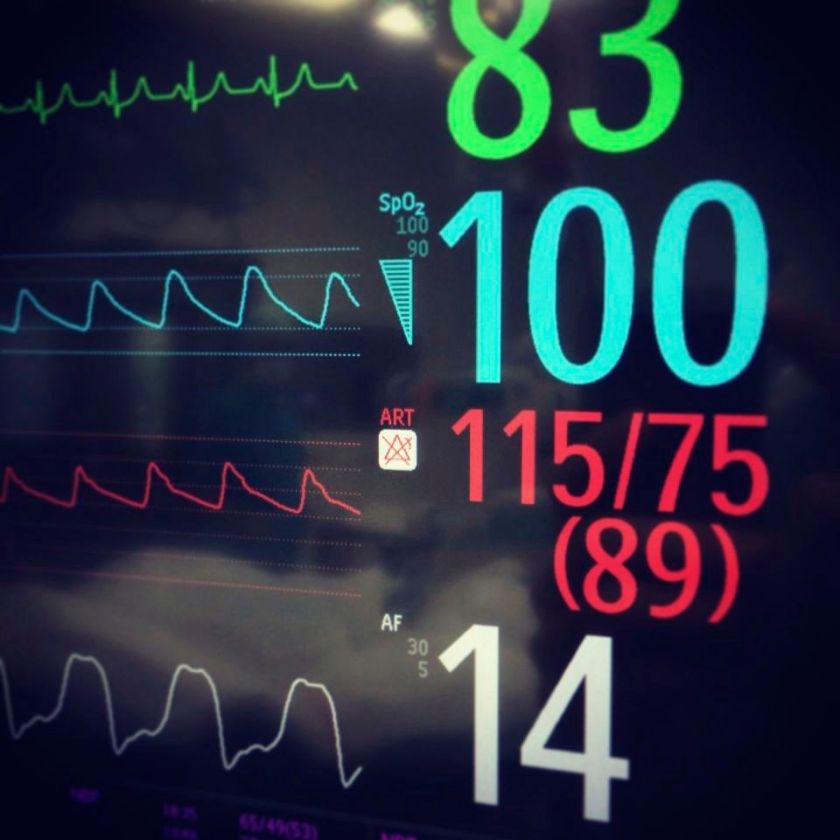
Das Monitoring zeigt folgende Parameter:
- SpO2: 78%, jedoch schwaches Pulsoxysignal (auch nach Lagewechsel zum Ohr)
- HF: 150/min.
- RR: 85/60 mmHg
- Monitor: rh., tc., QRS schmal
Das ABCDE-Schema ist wie folgt:
- A: frei, Mund trocken, Foetor ex ore
- B: Tachypnoe (30/min.), periphere Zyanose, Pulmo: leises exsp. Giemen global bds.
- C: A. rad. schwach tastbar, Rekap.: 4 sek., Cor: rh., tc., HT rein, Haut: kalt, blass, exsikkotisch
- D: Initial somnolent, GCS 11 (3/3/5), alle 4 Extr. frei beweglich, kein Meningismus, kein Secessus (akut), kein Zungenbiss, Babinski bds. neg., Pupillen bds. rund, isokor, lichtreagibel, eng
- E: Geschwollenes li. Ohr + li. Hand, zentralisiert, stammbetonte, wegdrückbare, münzgroße Makulae (lt. Mutter neu), Abd. weich, keine Beinödeme, keine sichtbaren Punktionsstellen, 36,7 Grad C, BZ: 130 mg/dl, keine sichtbaren Verletzungszeichen, keine Einstichstellen, qSOFA 3
Ein 12-K-EKG zeige keine wesentlichen Veränderungen (SR, rh, tc, ST, P unauffällig, PQ 120 msek., QRS schmal, R/S: V4/V5, keine ERBST, QT normal)
Der Patient zeigt also deutliche Zeichen eines Schocks und hat primär ein B- und C- Problem. Aufgrund der gefundenen Vitalparameter und der unklaren Ätiologie entscheiden wir uns dazu einen Notarzt nachzufordern, einen peripheren Zugang zu legen und den Patienten mit Sauerstoffgabe ins Auto zu bringen um ihn besser beurteilen zu können. Nach drei Versuchen eine Leitung zu etablieren gelingt es am Handrücken der li. (gschwollenen) Hand. Der Patient wird mit dem Rettungstuch aufgrund der engen Gegebenheiten aus der Wohnung getragen und wird dabei zunehmend agitierter, schlägt mit Armen und Beinen um sich. Eigentlich wollen wir den Patienten daher ein wenig beruhigen und Dormicum verabreichen, allerdings entfernt er sich bereits zuvor die Leitung durch seine Bewegungen selbst.
Im Auto angekommen erfolgt eine Revaluierung und ein erneuter Leitungsversuch. Wir haben uns dazu entschlossen eine Leitung zu legen, Volumen (Elo-iso) zu geben, eine art. BGA zu machen und Dormicum (initial 3 mg) zu applizieren. Dieser Plan wird umgesetzt und die art. BGA ergibt folgendes:
- pH 7,02
- pCO2 69 mmHg
- pO2 79 mmHg
- BE -15,5
- HCO3– 17,3 mmol/l
- Na+ 148 mmol/l
- K+ 5,4 mmol/l
- Cl– 116 mmol/l
- AL 20,1
Man sieht also eine gemischte resp. Azidose und eine high anion gap metabolic acidosis (HAGMA), außerdem eine resp. Partialinsuff.
Aufgrund der Zusammenschau von Klinik und Parametern entscheiden wir uns dazu den Patienten zu narkotisieren und endotracheal zu intubieren. Wir beginnen den Sauerstoff aufzudrehen um ihn gut zu präoxygenieren, außerdem legen wir eine Arterie. Die Narkose leiten wir mit folgenden Medikamenten ein:
- Dormicum 10 mg i.v.
- KetanestS 50 mg i.v.
- Esmeron 100 mg i.v.
Nach der Applikation von Esmeron fällt uns plötzlich proximal der Leitung eine Schwellung auf, die zuvor unerkannt blieb, da die Leitung in der li. Cubita und damit auf der geschwollenen Extremität lag. Stress bricht aus, da das die einzige Leitung ist, wir nicht wissen wie viel Esmeron bereits para gelaufen ist und falls der Patient mit dem Blutdruck abfällt oder das Esmeron nicht ausreichend angekommen ist, der Patient aber zu Atmen aufhört – wir keine optimalen Intubationsbedingungen vorfinden hätten können. Daher entschließen wir uns dazu einen neuen Zugang zu legen. Einerseits wird der Knochenbohrer hergerichtet und andererseits inzwischen versucht die Jugularis ext. zu punktieren – was auch auf Anhieb gelingt. Der Patient atmet immer noch spontan, der Kreislauf ist stabil. Daraufhin erhält der Patient dieselbe Narkose wie oben erwähnt in derselben Dosierung.
Die Atemwegssicherung geschieht folgendermaßen:
- ID: 7,5 mm
- ZR: 22 cm
- VA bds.
- Kapno 33 mmHg
Anschließend erfolgt eine erneute kurze Revaluierung und der Transport ins vorangekündigte Krankenhaus (LKH Süd-West, Standort Süd, Graz). Auf dem Transport wird der Patient kurzzeitig hypoton sodass 10 mg Ephedrin verabreicht werden, anschließend verläuft der Transport komplikationslos.
Im Krankenhaus wird der Patient übergeben und beim Ummonitorisieren fällt uns beim anderen Monitor plötzlich eine massive ST-Hebung in II auf. Der diensthabende FA meint, dass das aussieht wie ein STEMI und will gerade einen Ultraschall machen als der Patient plötzlich bradykard wird. Es endet in einem AVB III Grades ohne Ersatzrhythmus und damit in der CPR. Die art. BGA wird wiederholt und aufgrund einer massiven Hyperkaliäme (6,7 mmol/l) NaBi verabreicht, woraufhin ein ROSC entritt.
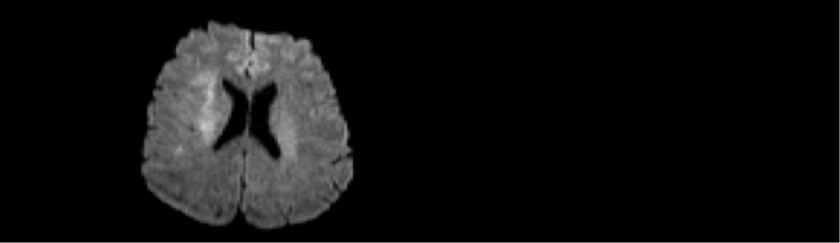
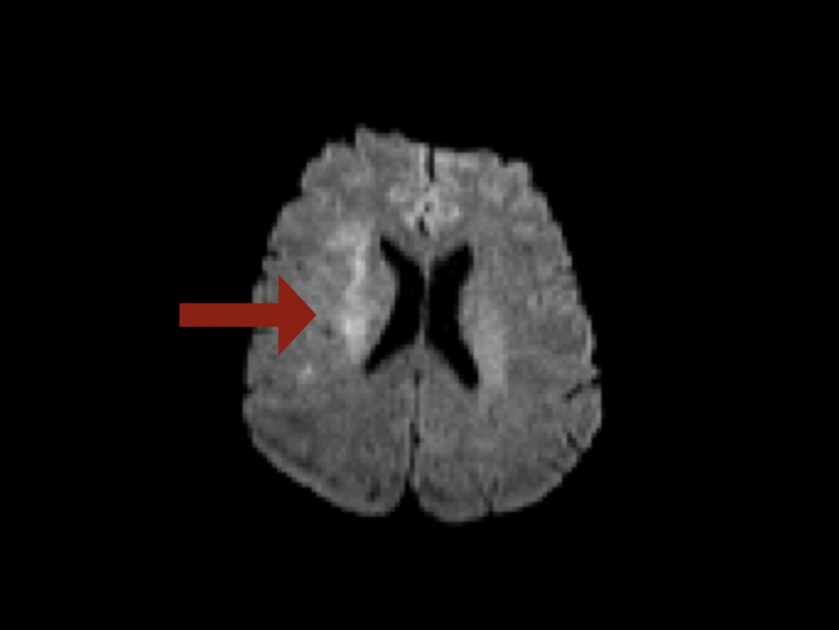
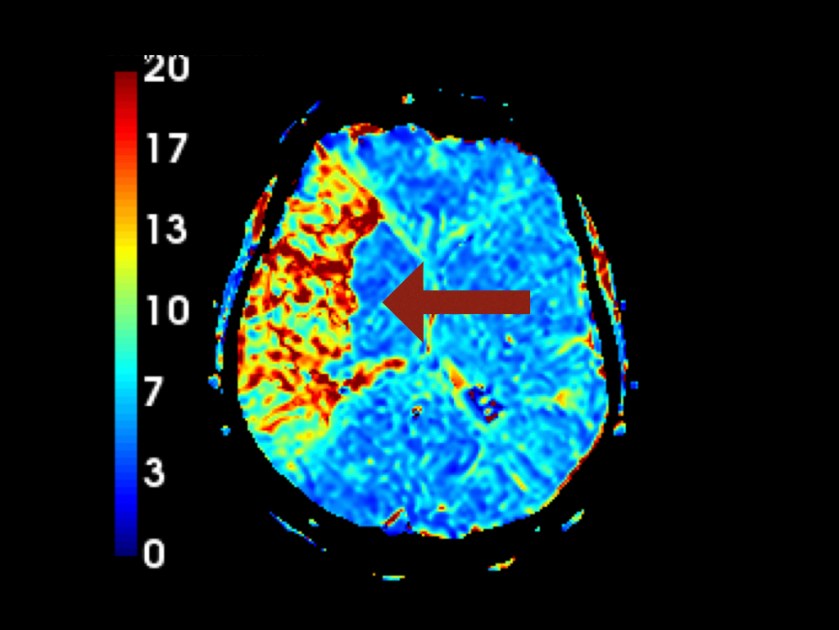
Letztendlich hat der Patient nach einem langen Krankenhausaufenthalt wieder ein „normales“ Leben aufgenommen. Es hat sich herausgestellt, dass er „Angel Dust“ inhaliert hat, woraufhin eine Rhabdomyolyse folgte, ein hypovolämischer Schock und eine myoglobinurische Acute Kidney Injury, die zur Hyperkaliämie führte, da sich eine Crush-Niere entwickelt hat.
Was hätte man verbessern können:
- Zeit: die Patientenversorgung nahm 1,5 h in Anspruch – großteils durch Komplikationen verursacht, die viel Zeit beansprucht haben
- Sicherungsleitung: in diesem Fall war es schwer diese eine zu legen, die gerade im ungünstigsten Augenblick nicht mehr funktionierte. Das wäre vermeidbar gewesen, wenn eine Checkliste verwendet worden wäre, wo 2 Leitungen fix gefordert werden und dann hätte man direkt zum Bohrer gegriffen. Diese lag zwar bereit, wurde jedoch nicht detailiert abgearbeitet.
Ich stellte mir vor Ort regelmäßig die Frage, warum ein gesunder, junger Mensch einen derartigen Schock entwickelt. Für mich lag die Sepsis nahe, besonders mit der Drogenvorgeschichte im Hintergrund, auch wenn die Peripherie nicht überperfundiert war. Man muss aber auch sagen, dass diese Überlegung meiner Meinung zwar wichtig ist um optimalerweise kausal therapieren zu können, sie hat aber für das Management keine Rolle gespielt, denn der Patient hätte auf jeden Fall derartige Interventionen gebraucht. Dieses Beispiel ist nicht nur spannend, weil es nicht besonders oft vorkommt, sondern vor allem auch, weil man zwar dabei etwas ratlos ist, durch strukturiertes Abarbeiten des ABCDE-Schemas jedoch trotzdem den Patienten gut versorgen kann. Es zeigt außerdem, dass man oft glaubt keine Zeit für „Kleinigkeiten“ – wie eine Checkliste durchzugehen – zu haben, da man unter Stress steht. Hier sieht man ganz gut, dass man andernfalls jedoch noch mehr Stress produziert und damit Fehler passieren können, die vermeidbar sind.
Dieses Fallbeispiel wurde auch im Rahmen eines Jour-fix der steirischen Arbeitsgemeinschaft Notfallmedizin AGN (www.agn.at) präsentiert, ein Video davon ist auf YouTube am sehr empfehlenswerten Channel der AGN verfügbar!